사업영역
CMO & CDMO
Contract Development and Manufacturing Organization
(임상시험용)의약품 GMP 제조
-
→ 유전자재조합 기반의 cGMP 제조시설 및 풍부한 업무경험 보유
- ∙ 임상시험용)의약품 cGMP 제조 적합시설(2020년 인증 예정)
- ∙ 소용량 및 대용량 생산에서 재현 가능한 생산 공정 개발
- ∙ 미생물배양 기반 바이오의약품의 (임상시험용)의약품 cGMP 제조 및 제조공정 기술 보유
- ∙ 액상주사제, 동결건조주사제의 (임상시험용)의약품 cGMP 제조 및 제조공정 기술 보유
- ∙ 국내/외 규제기관의 실사 경험을 보유한 QA 전문인력 보유
- ∙ cGMP, EU-GMP, KGMP의 규정과 ICH 지침을 포괄하는 Quality program(Quality system, Facilities & Equipment, Materials, Productions, Packaging & Labeling, Laboratory control) 보유
- ∙ cGMP 제조소 : Grade A/B(무균시설), Grade C/D(미생물관리구역), CNC(Controlled not classified)

∙ 유전자재조합 기반의 바이오의약품 개발 프로세스
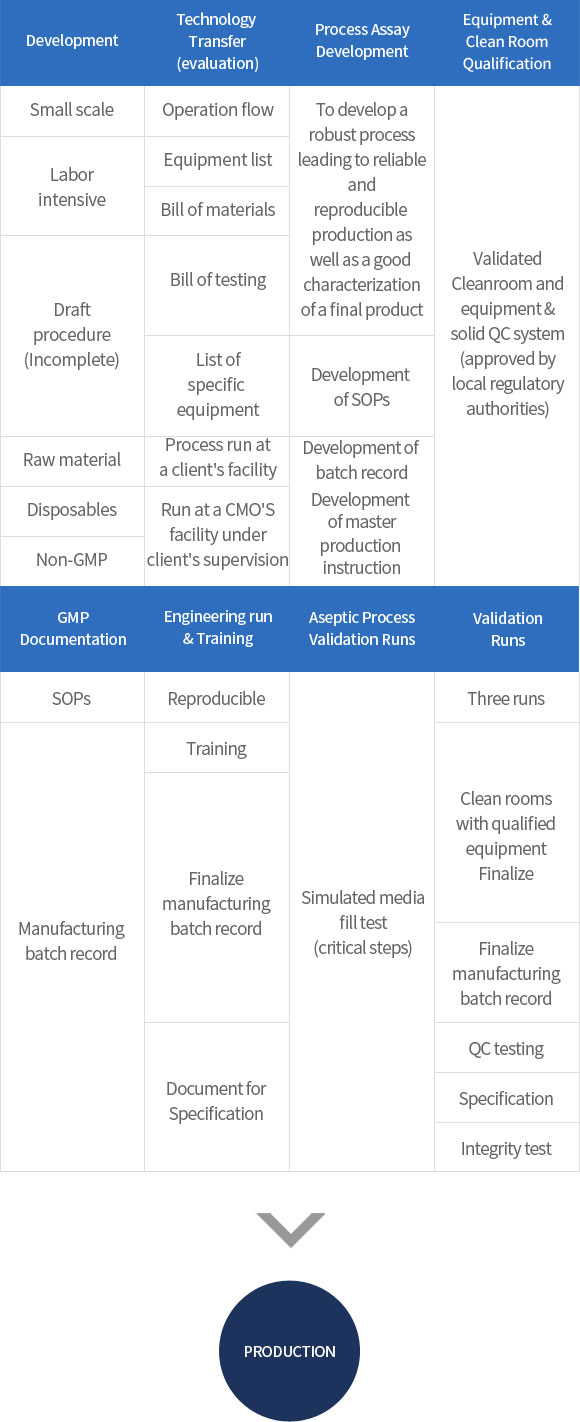
∙ 유전자재조합 원료의약품 및 완제의약품의 (임상시험용)바이오의약품에 대한 GMP 제조공정 및 밸리데이션 서비스 제공
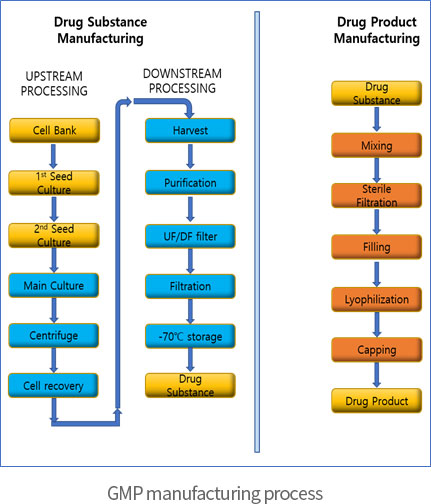
비임상 Non-GMP 제조
-
→ 미생물배양 기반 유전자재조합 바이오의약품의 DS, DP에 대해개발 초기단계부터 R&D 및 비임상시험용의약품의 생산 서비스 제공
- ∙ 유전자재조합 세포주(E.coli) 배양 및 정제 공정
- ∙ 액상주사제 및 동결건조주사제
- ∙ 분석법 개발(Identity, Quantity, Potency, Impurities)

Custom Services
-
→ 바이오의약품 원료 및 완제의약품 제조공정 개발 등 Custom Services
- ∙ 유전자재조합 의약품에 사용되는 세포주 스크리닝
- ∙ 사용자 요구수준을 만족하는 배양조건 및 정제조건 개발
- ∙ Drug Substance 배양 및 정제공정의 최적화
- ∙ 밸리데이션(Validation) 및 인허가(Regulatory Affairs) 서비스 전문기업
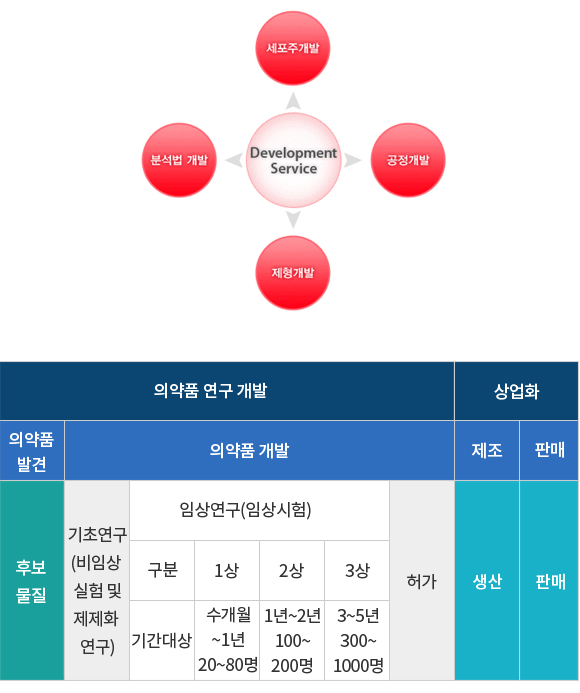
-
→ 배양공정개발
- ∙ 세포배양 조건 개발 및 개선
- ∙ 배양공정개발: Batch, Fed-batch, seed culture
- ∙ Drug Substance 배양 및 정제공정의 최적화
- ∙ 밸리데이션(Validation) 및 인허가(Regulatory Affairs) 서비스 전문기업
-
→ 정제공정개발
- ∙ 공정 개선 및 최적화
- ∙ Purification process개발
- ∙ UF/DF membrane의 type & sizing 시험
- ∙ 정제공정 셋업
-
→ 스케일업 연구
- ∙ 50 L/500 L 규모 공정 셋업 및 분석
- ∙ (비)임상시료 생산을 위한 공정이전
-
→ 제형개발 연구
- ∙ 단백질, 부형제물 조성을 위한 제형개발을 통해 제품의 특성 및 안정성 최적화
- ∙ 액상주사제 및 동결건조주사제 제형 개발

-
→ 분석법 개발/지원
- ∙ 제품별 특성에 적합한 분석법 개발(Identity, Quantity, Purity, Potency, Impurities, Endotoxin, Physico-chemical tests)
- ∙ 분석법 밸리데이션(Specificity, Accuracy, Precision, Detection Limit, Quantitation, Limit, Linearity, Range, Robustness)
- ∙ 안정성 시험(stability test) 연구
-
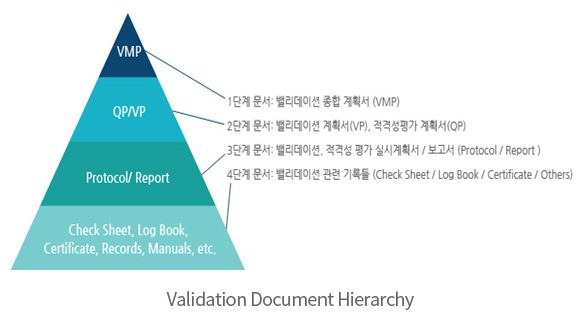
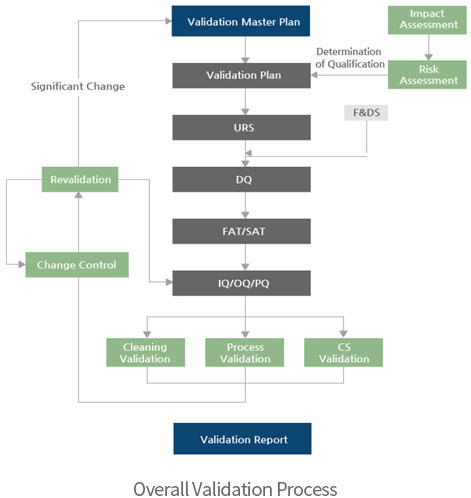
→ 밸리데이션
- ∙ 밸리데이션(Validation)/적격성평가(Qualification) 가이드라인에 규정된 절차 수행
-
∙ 밸리데이션(Validation)
- - 공정 밸리데이션(Process Validation, PV)
- - 세척 밸리데이션(Cleaning Validation, CV)
- - 컴퓨터 시스템 밸리데이션(Computer System Validation, CSV)
-
∙ 적격성평가(Qualification)
- - 시스템영향평가(System Impact Assessment, SIA))
- - 위험평가(Risk Assessment, RA)
- - 사용자요구규격서(User Requirements Specification, URS))
- - 설계적격성평가(Design Qualification, DQ)
- - 공장검수(Factory Acceptance Test, FAT)
- - 현장검증(Site Acceptance Test, SAT)
- - 설치적격성평가(Installation Qualification, IQ)
- - 운전적격성평가(Operational Qualification, OQ)
- - 성능적격성평가(Performance Qualification, PQ)
-
적격성평가 대상
- - 적격성평가 계획(Qualification Planning)
- - 생산장비 및 건축설비 적격성평가(Process Equipment and Utilities)
- - 용수 제조 및 분배시스템(Water Generation and Distribution System): 정제수(Purified Water), 주사용수(Water For Injection), 청정스팀(Clean Steam)
- - 공기조화장치(HVAC System)
- - 압축공기시스템(Compressed Air System)
- - 크린룸(Clean Room)
- - 컴퓨터 및 자동화시스템(Computer and Automation System)
GMP 제조소 (오송 바이오플랜트)
-
→ 면적
- ∙ 약 6000평(19,932 m2)
-
→ 시공 스케줄
- ∙ 2020년 2사분기 완공 예정
-
→ GMP 제조 시설
- ∙ 원자재 보관소(검체채취실, 칭량실 포함)
- ∙ 완제의약품 보관소(저온실)
- ∙ 원료의약품 제조라인(미생물 발효, 정제)
- ∙ 완제의약품 제조라인(무균주사제, 동결건조주사제)
- ∙ 포장실(자동이물검사기, 라벨러, 포장라인)
- ∙ QC시험실(칭량실, 이화학시험실, 미생물시험실, 안정성/보관검체실)
- ∙ 기계실(용수제조장치, 공기조화장치, 압축공기제조장치 등)
-
→ 활용계획
- ∙ (비)임상시험용의약품 제조
- ∙ 상업용의약품 제조
- ∙ C(D)MO 사업
-
→ 목표 GMP 수준
- ∙ cGMP, EU GMP, KGMP 등 글로벌 GMP 준수



